CAR-T技术的成功,让基因编辑的免疫细胞治疗成为了可能。在这样的背景下,将NK细胞进行编辑获得的CAR-NK也成了人们关注的热点。
什么是NK细胞
NK细胞全称自然杀伤细胞,具有细胞毒性和免疫调节双重功能。和T细胞一样,NK细胞表面有众多受体,分为激活性和抑制性受体两类,当NK细胞与健康细胞接触时,健康细胞的的MHC分子会激活NK的抑制性受体,避免NK细胞的激活对健康细胞的误伤。但是,当NK细胞接触到MHC分子下调的肿瘤细胞时,由于抑制信号的缺失可引起NK细胞对肿瘤的杀伤。同时,当某些肿瘤细胞激活信号的上调也会引起NK细胞的激活和对肿瘤细胞的杀伤。总而言之NK细胞是人体内抗癌防线不可或缺的组成部分,直接参与人体对肿瘤细胞的杀伤过程。
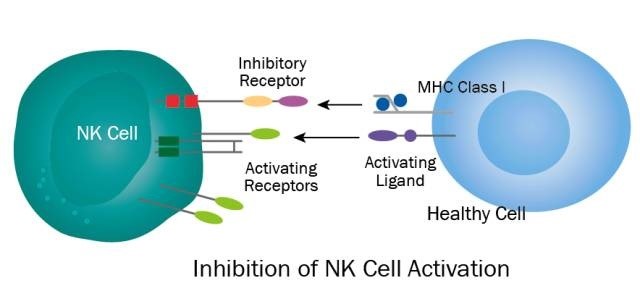
图示说明:健康细胞表面的MHC分子激活了NK细胞上的抑制性受体,抑制的NK细胞的激活
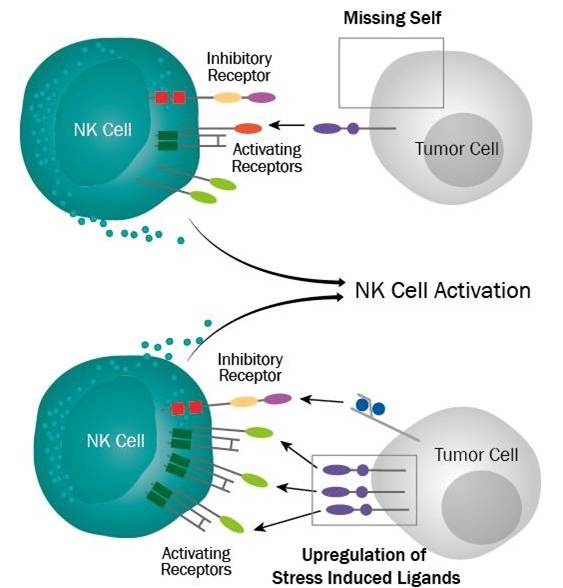
图示说明:当肿瘤细胞表面的MHC分子丢失或者上调激活信号时,可以激活NK细胞对肿瘤的杀伤。
CAR-NK的特点
正是因为NK细胞在抗肿瘤领域扮演着重要的角色,因此CAR技术的发展也催生了CAR-NK的诞生。经过CAR结构修饰后的NK细胞,理论上也能够高效的识别肿瘤细胞,并通过释放杀伤介质、诱导靶细胞凋亡等多种手段杀伤肿瘤细胞。但相对于CAR-T,由于NK细胞的天然特性,CAR-NK的治疗过程中不会产生严重的细胞因子风暴,因此在临床使用中,安全性可能较CAR-T更高。其次,由于NK细胞在体内的存活时间较T细胞更短,导致CAR-NK在体内的存活时间较CAR-T更短。这一特性或许会导致CAR-NK细胞疗效不如CAR-T,但是从安全性的角度来说,这种特性反而避免了经过基因修饰的免疫细胞长期存在于人体可能导致的一系列未知的风险。
和T细胞相比,目的基因导入NK细胞具有更大的挑战性,因此其开展的临床实验要远低于CAR-T和TCR-T,但无论如何,CAR-NK也将会是肿瘤免疫治疗领域发展的新方向。
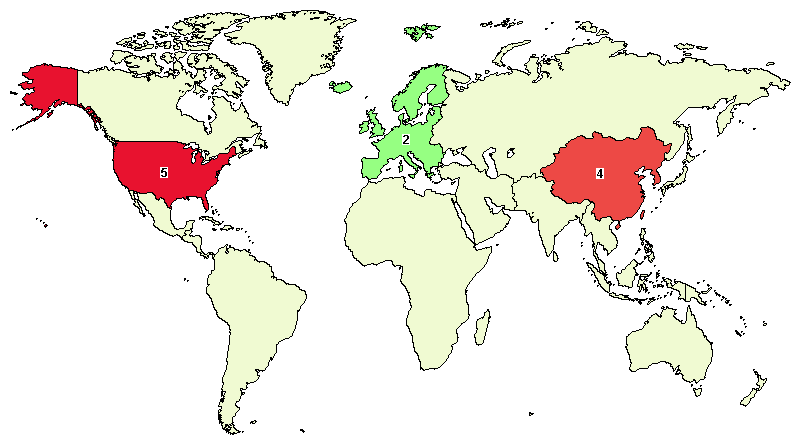
截至2018年6月,全球开展的CAR-NK临床数量要远低于CAR-T的临床数量
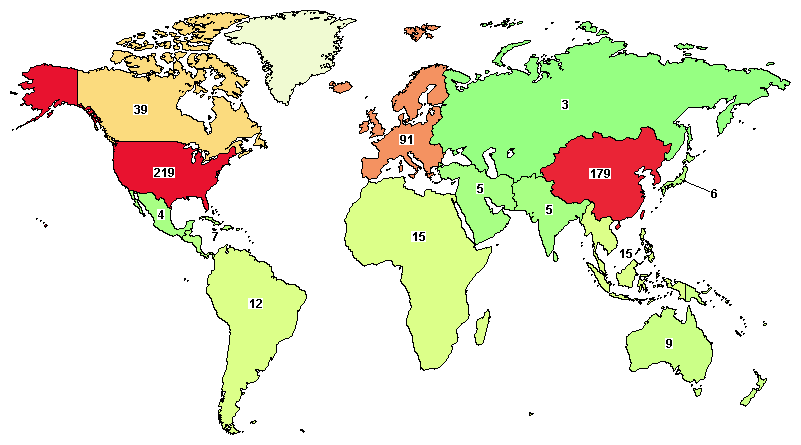
截至2018年6月,全球开展的CAR-T临床分布